1. Pengelompokan Unsur Menurut Lavoisier
Pada 1789, Antoine Lavoiser mengelompokan 33 unsur kimia. Unsur-unsur kimia di bagi menjadi empat kelompok, yaitu :
- Unsur gas cahaya, kalor, oksigen, azote ( nitrogen ), dan hidrogen.
- Unsur non logam sulfur, fosfor, karbon, asam klorida, asam flourida, dan asam borak.
- Unsur logam antimon, perak, arsenik, bismuth. Kobalt, tembaga, timah, besi, mangan, raksa, molibdenum, nikel, emas, platina, tobel, tungsten, dan seng.
- unsur tanah kapur, magnesium oksida, barium oksida, aluminium oksida, dan silikon oksida.
Kelemahan dan kelebihan sistem periodik unsur Lavoisier :
- Kelemahan dari teori Lavoisior : Penglompokan masih terlalu umum
- Kelebihan dari teori Lavoisior : Sudah mengelompokan 33 unsur yang ada berdasarka sifat kimia sehingga bisa di jadikan referensi bagi ilmuan-ilmuan setelahnya Dobereiner mengelompokan setiap tiga unsur kimia yang sifatnya mirip dengan satu kelompok berdasarkan kenaikan berat atomnya. Lebih dikenal dengan Hukum Triade Dobereiner.Kelemahan dari teori ini adalah pengelompokan unsur ini kurang efisian dengan adanya beberapa unsur lain dan tidak termasuk dalam kelompok triad padahal sifatnya sama dengan unsur dalam kelompok triad tersebut.Kelebihan dari teori ini adalah adanya keteraturan setiap unsur yang sifatnya mirip massa Atom (Ar) unsur yang kedua (tengah) merupakan massa atom rata-rata di massa atom unsure pertama dan ketiga
- 3. Newland (John Alexander Reina Newland)Newland mengelompokkan berdasarkan kenaikan berat atom. Sifat-sifat unsur akan berulang pada unsur kedelapan, sehingga unsur pertama akan sama sifatnya dengan unsur kedelapan. Dikenal dengan Teori Oktaf.Mendeleev mengatakan bahwa jika unsur disusun menurut massa atom yang meningkat, maka unsur-unsur dengan sifat yang sama akan tersusun secara periodik.
- Sifat kimia dan fisika unsur dalam satu golongan mirip dan berubah secara teratur.
- Valensi tertinggi suatu unsur sama dengan nomor golongannya.
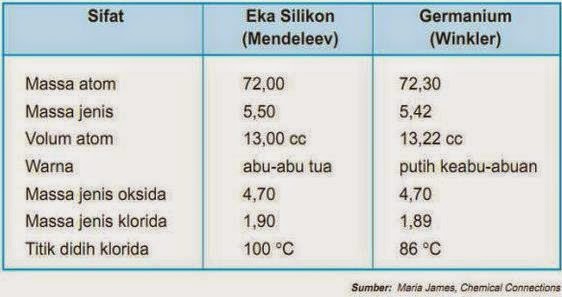
- Dapat meramalkan sifat unsur yang belum ditemukan pada saat itu dan telah mempunyai tempat yang kosong.
b. Kekurangan / Kelemahan sistem periodik Mendeleev- Panjang periode tidak sama dan sebabnya tidak dijelaskan.
- Beberapa unsur tidak disusun berdasarkan kenaikan massa atomnya, contoh : Te (128) sebelum I (127).
- Selisih massa unsur yang berurutan tidak selalu 2, tetapi berkisar antara 1 dan 4 sehingga sukar meramalkan massa unsur yang belum diketahui secara tepat.
- Valensi unsur yang lebih dari satu sulit diramalkan dari golongannya.
- Anomali (penyimpangan) unsur hidrogen dari unsur yang lain tidak dijelaskan.
5.Sistem Periodik Modernpada tahun 1914, Henry G. J. Moseley menemukan bahwa urutan unsur dalam tabel periodik sesuai kenaikan nomor atom. Tabel periodik modern yang disebut juga tabel periodik bentuk panjang, disusun menurut kenaikan nomor atom dan kemiripan sifat. Tabel periodik modern ini dapat dikatakan sebagai penyempurnaan Tabel Periodik Mendeleyev.- Golongan
Golongan adalah susunan unsur-unsur dalam SPU ke arah tegak (vertikal) yang disusun berdasarkan kemiripan sifat. Secara garis besar unsur-unsur dalam Tabel Periodik Modern dibagi dalam 2 golongan, yaitu:
Golongan Utama (A), meliputi:
- Golongan IA disebut golongan alkali;
- Golongan IIA disebut golongan alkali tanah;
- Golongan IIIA disebut golongan boron/aluminium;
- Golongan IVA disebut golongan karbon/silikon;
· - Golongan VA disebut golongan nitrogen/fosfor;
- Golongan VIA disebut golongan oksigen/sulfur;
- Golongan VIIA disebut golongan halogen;
- Golongan VIIIA/O disebut golongan gas mulia/gas inert.
Golongan Transisi (B), meliputi:
- Golongan Transisi (Gol. B), yaitu : IIIB, IVB, VB, VIB, VIIB, VIIIB (VIII), IB, dan IIB.
- Golongan Transisi Dalam, ada dua deret. Pada periode 6 golongan IIIB terdapat 14 unsur yang sangat mirip sifatnya, yaitu unsur-unsur Lantanida. Demikian juga pada periode 7 yaitu unsur-unsur Aktinida. Supaya tabel tidak terlalu panjang, unsur-unsur tersebut ditempatkan tersendiri pada bagian bawah sistem periodik.· Periode
Periode adalah susunan unsur-unsur dalam SPU arah mendatar (horizontal) yang disusun berdasarkan kenaikan nomor atom. Periode dibagi 2 yaitu:
Periode pendek, meliputi:
- Periode 1 terdiri atas 2 unsur;
- Periode 2 terdiri atas 8 unsur;
- Periode 3 terdiri atas 8 unsur.
Periode panjang, meliputi:
- Periode 4 terdiri atas 18 unsu;
- Periode 5 terdiri atas 18 unsur;
- Periode 6 terdiri atas 32 unsur.- Periode 7 belum lengkap -
- Mudah dibaca dan dipahami.
- Strukturnya jelas dan tertata dengan lebih baik.
- Menyisakan tempat bagi unsur-unsur yang belum ditemukan
- Berhasil menyusun golongan transisi dalam yang terdiri dari Lantanida dan Aktinida, dimana Aktinida diletakkan di bawah Lantanida
Kekurangan / Kelemahan Sistem Periodik Seaborg :- Belum ada kekurangan yang baik pada susunan tabel maupun peletakan setiap unsurnya sehingga tabel periodik terus digunakan sampai sekarang.
Semoga bermanfaat, Akhirul Qalam Assalamualaikum wr wb - @fajarrahman89




0 Response to "Kelebihan dan kekurangan masing-masing teori tabel periodik"
Post a Comment